Bestemmelse af antallet af neutroner i et atom er faktisk ret simpelt og kræver ikke engang nogen eksperimenter. For at beregne antallet af neutroner i en almindelig atom eller en isotop, følge disse instruktioner.
Steps
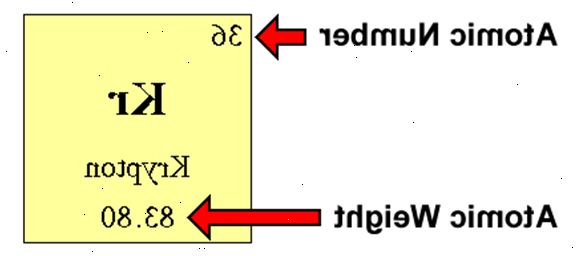
Neutroner i en regelmæssig atom
- 1Find element på det periodiske system. I dette eksempel vil vi se på osmium (Os), som er i den sjette række ned.
- 2Find elementets atomnummer. Denne tendens til at være den mest synlige tal vedrørende et bestemt element, og som regel sidder over elementet symbol. (På vores eksempel diagram, i virkeligheden er der ikke andre numre på listen.) Atomnummeret er antallet af protoner i et enkelt atom af dette element. Os er nummer 76, hvilket betyder et atom af osmium har 76 protoner.
- 3Find elementets atomvægt. Dette nummer er normalt findes under den atomare symbol. (Bemærk, at diagrammet i dette eksempel er udelukkende baseret på atomnummer og ikke liste atomvægten. Dette vil normalt ikke være tilfældet.) Osmium har en atomvægt på 190,23.
- 4Afrund atomvægt til det nærmeste hele tal for at finde den atomare masse. I vores eksempel, ville 190,23 afrundes til 190, hvilket resulterer i en atommasse på 190 for osmium.
- 5Fratræk atomnummer fra atommassen. Da størstedelen af atomets masse fundet sin protoner og neutroner, trække antallet af protoner (dvs. atomnummer) fra atommassen vil give dig det beregnede antal neutroner i atomet. I vores eksempel, er dette: 190 (atomvægt) - 76 (antal protoner) = 114 (antal neutroner).
- 6Husk formlen. For at finde antallet af neutroner i fremtiden, skal du blot bruge denne formel:
- N = M - N
- N = antal N eutrons
- M = atomic M røv
- n = atomare n umbra
- N = M - N
Neutroner i en isotop
- 1Find element på det periodiske system. Som et eksempel, vil vi se på kulstof-14 isotop. Eftersom den ikke-isotop form af kulstof-14 er simpelthen kulstof (C), find carbon på den periodiske tabel (i anden række ned).
- 2Find elementets atomnummer. Denne tendens til at være den mest synlige tal vedrørende et bestemt element, og som regel sidder over elementet symbol. (På vores eksempel diagram, i virkeligheden er ingen andre numre anført.) Atomnummeret er antallet af protoner i et enkelt atom af dette element. C er nummer 6, hvilket betyder et atom af kulstof har 6 protoner.
- 3Find den atomare masse. Det er utroligt nemt med isotoper, som de er opkaldt efter deres atommasse. Kulstof-14, for eksempel, har en atommasse på 14.
- 4Fratræk atomnummer fra atommassen. Da størstedelen af atomets masse fundet sin protoner og neutroner, trække antallet af protoner (dvs. atomnummer) fra atommassen vil give dig det beregnede antal neutroner i atomet. I vores eksempel, er dette: 14 (atommasse) - 6 (antal protoner) = 8 (antal neutroner).
- 5Husk formlen. For at finde antallet af neutroner i fremtiden, skal du blot bruge denne formel:
- N = M - N
- N = antal N eutrons
- M = atomic M røv
- n = atomare n umbra
- N = M - N
Tips
- Protoner og neutroner udgør næsten hele vægten af de elementer, mens elektroner og diverse partikler repræsenterer ubetydelig masse (nærmer sig nul masse). Da en proton har omtrent samme vægt som en neutron og atomnummer repræsenterer antallet af protoner, kan vi simpelthen trække antallet af protoner fra den samlede masse.
- Osmium, et metal, der er fast ved stuetemperatur, navn stammer fra det græske ord for lugt, "osme".
- Hvis du nogensinde i tvivl, hvilket nummer er som i en periodisk tabel, bare huske at tabellen normalt er designet omkring det atomnummer (dvs. antal protoner), der starter ved 1 (brint) og bestiger en enhed ad gangen fra venstre til højre ved 118 (Ununoctium) slutter. Dette skyldes, at antallet af protoner i et atom bestemmer, hvad der atom er, hvilket gør det lettest elementært træk at organisere ved. (Eks. et atom med 2 protoner er altid helium, ligesom et atom med 79 protoner er altid guld.)
